近年来,肥胖日益成为一个全球性疾病,引起糖尿病、脂肪肝、心血管疾病等多种代谢并发症,对人类健康带来巨大危害。根据代谢特征,脂肪细胞可以分为白色、米色和棕色脂肪细胞三类。白色脂肪细胞用来储存能量,而米色和棕色脂肪细胞(统称为产热脂肪细胞)能够消耗能量,以热能的形式释放,其分化异常和产热功能受损在肥胖的发生发展过程中发挥重要作用。谷氨酰胺是人体内重要的非必需氨基酸,在体内参与氮循环、细胞增殖、激活自噬等生物过程,在体内可以由谷氨酸与氨经谷氨酰胺合成酶Glul催化而成。过去研究提示谷氨酰胺为肥胖的保护因子,然而Glul/谷氨酰胺在产热脂肪细胞分化及功能中的作用及其潜在作用机理仍知之甚少,有待深入解析。
2023年8月14日,浙江大学基础医学院孟卓贤研究员团队和浙江大学医学院附属第二医院单鹏飞主任团队合作在《Diabetes》杂志在线发表题为“Glutamine production by Glul promotes thermogenic adipocyte differentiation through Prdm9-mediated H3K4me3 and transcriptional reprogramming” 的研究论文,发现并揭示了谷氨酰胺通过Prdm9介导的组蛋白修饰和转录重编程调控产热脂肪细胞分化。

该研究首先通过分析人腹股沟皮下脂肪的基因表达谱和氨基酸代谢相关基因的组织分布图谱,筛选得到一个在超重和肥胖患者的皮下脂肪中显著下调,且在棕色脂肪中特异性高表达的基因Glul(图1)。
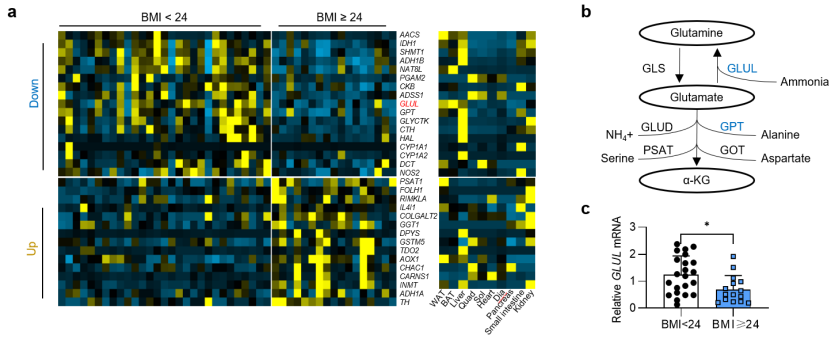
图1 GLUL在超重和肥胖患者的腹股沟皮下脂肪组织中显著低表达
进一步利用肥胖和2型糖尿病(T2D)小鼠模型的脂肪样本,作者发现Glul在肥胖和T2D小鼠棕色脂肪中显著低表达。为了进一步研究Glul与脂肪组织产热之间的联系,研究人员在冷刺激小鼠模型和β3肾上腺素受体激动剂Cl316,243刺激小鼠模型中发现,Glul在脂肪组织中表达量显著增加,且Glul在棕色脂肪细胞系BAC分化过程中表达量逐渐升高。这些结果提示Glul及其产物谷氨酰胺可能在产热脂肪细胞的分化、功能调控以及肥胖的发生发展中发挥重要作用。
为了探究Glul/谷氨酰胺对棕色脂肪细胞分化和功能的影响,研究人员采用了CRISPR/Cas9技术设计gRNA靶向Glul基因在BAC中实现敲除。在去除外源性培养基中的谷氨酰胺后,Glul敲除的BAC细胞无法正常分化,且其产热功能被显著抑制。作者同时也使用Glul酶活性抑制剂MSO在BAC中进行了处理,发现与Glul敲除细胞系结果一致。为了进一步研究谷氨酰胺是影响成脂还是产热本身,作者在白色脂肪细胞系3T3L1和成熟的BAC细胞中进行了MSO处理和外源性谷氨酰胺的去除,发现3T3L1细胞在无谷氨酰胺的情况下同样无法分化,而分化成熟的BAC在无谷氨酰胺的情况下其产热功能被明显抑制,提示了谷氨酰胺对脂肪细胞产热功能的调控独立于其对细胞分化的影响。
机制研究方面,研究人员借助RNA-Seq,ATAC-Seq和CUT&Tag-Seq三种高通量测序方法对Glul敲除的BAC细胞进行联合分析,发现谷氨酰胺通过调控H3K4me3和Acetyl-H3组蛋白修饰从而影响染色质开放性,促进成脂和产热基因的表达。进一步通过检测BAC分化过程中组蛋白修饰酶的变化,筛选并通过基因敲降验证,发现Prdm9在棕色脂肪中特异性高表达,敲除Prdm9基因显著抑制BAC的成脂及产热功能(图2)。
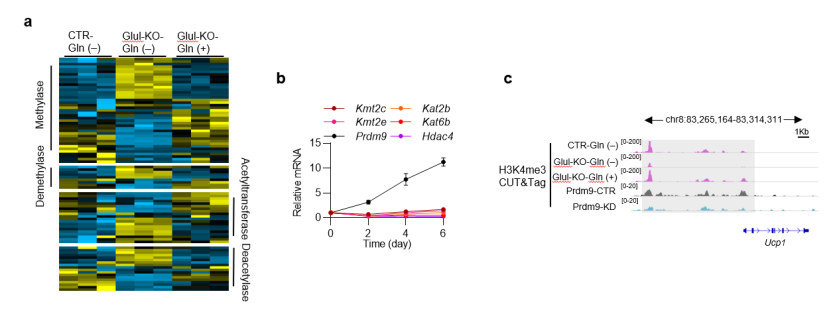
图2 谷氨酰胺通过Prdm9影响棕色脂肪细胞分化的筛选及验证
进一步通过对在BAC中受到Glul/谷氨酰胺调控的ATAC-Seq序列进行基序分析,结合荧光素酶报告基因实验和脂肪细胞内基因敲降等方法,作者发现谷氨酰胺可以通过增加转录因子C/EBPb在Prdm9基因增强子上的结合调控其转录。
为了探索谷氨酰胺对肥胖及其相关代谢性疾病的治疗作用和潜在临床价值,研究人员构建了Ala-Gln双肽补充小鼠模型。结果显示:灌胃或者饮水补充Ala-Gln能显著增强小鼠棕色脂肪的产热功能,改善高脂饮食诱导的肥胖和代谢紊乱。这些结果进一步验证了谷氨酰胺的产热代谢促进效应,并提示谷氨酰胺可作为肥胖和T2D的潜在治疗方法。
综上所述,该研究从人群样本出发,筛选并发现谷氨酰胺合成酶Glul在超重及肥胖患者皮下脂肪中显著低表达,进而从体内、体外两方面证明了谷氨酰胺通过促进棕色脂肪细胞分化和产热代谢,在全身糖脂代谢稳态调控中发挥重要作用。此外,该工作首次发现了谷氨酰胺通过C/EBPb/Prdm9通路调控组蛋白修饰和染色开放性影响棕色脂肪细胞成脂和产热基因表达(图3),为肥胖及其相关代谢性疾病的诊治提供了干预新靶点。
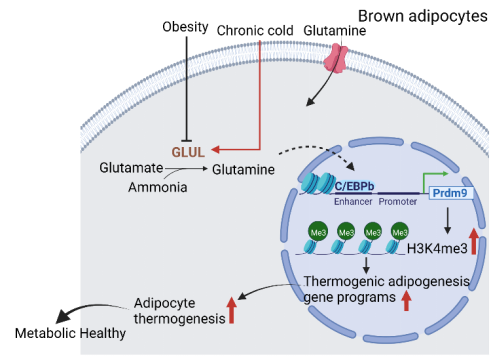
图3 Glul/谷氨酰胺调控产热脂肪分化、功能和全身代谢稳态模式图
浙江大学基础医学院孟卓贤研究员为论文的最后通讯作者,浙江大学附属第二医院单鹏飞主任为共同通讯作者。浙江大学医学院在读博士生潘晓闻、浙江大学附属第二医院叶凌霞主治医师为论文共同第一作者。该课题得到基础医学院的大力支持。研究获得国家自然科学基金、科技部国家重点研发计划、浙江省自然科学基金、浙江大学基础医学院原创探索培育计划项目等基金项目的资助。










