2008年北京和2012年伦敦奥运会上,我国著名跨栏运动员刘翔两度因伤退赛,职业生涯遭遇滑铁卢,并于多次手术中在肌腱中取出数块骨头。究其原因,这一切都是肌腱病惹的祸。这个疾病听起来似乎跟普通人距离很远,但实则不然。有研究统计,在运动系统疾病的临床咨询中,约有30%跟肌腱损伤有关。
肌腱是一种少细胞、乏血管组织,这样的构造赋予肌腱细胞能耐受日常活动的收缩牵拉,并造成缺氧的环境。但这个特性也是把双刃剑,会导致肌腱损伤后缺乏血供,影响愈合能力。因此,肌腱损伤若未及时发现并就诊,会逐渐发展成为慢性肌腱病。慢性肌腱病的临床主要表现为疼痛、肿胀以及活动障碍。肌腱病中存在一种特殊的类型——肌腱异位骨化。顾名思义,就是本不该出现骨头的地方(肌腱)中“长出”了骨头。这种在肌腱中的异常成骨会进一步破坏肌腱组织本身的形态构造,加剧症状和损害功能。
2020年4月29日,浙江大学基础医学院陈晓课题组、浙二肌腱病团队联合高分子系毛峥伟,浙江大学基础医学院周以侹教授共同在Science Advances杂志上发表了题为 Targeted pathological collagen delivery of sustained-release rapamycin to prevent heterotopic ossification的研究论文。该文章揭示了mTOR通路在调控肌腱异位骨化中的核心机制,并研发了一种能靶向病理肌腱的缓释递送雷帕霉素体系,用于预防肌腱异位骨化。
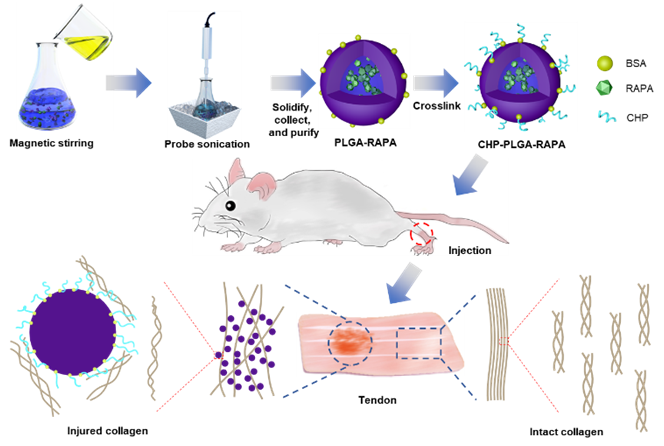
首先需要明白肌腱异位骨化形成的原因是什么。跟人体内的其他组织类似,肌腱中也存在着干/祖细胞。这类细胞在发育时分化为肌腱细胞,进一步分泌细胞外基质(胶原),形成肌腱组织。在肌腱成熟后,肌腱干/祖细胞保持在静息状态,维持组织的稳态。日积月累的超负荷工作会逐渐累积微小损伤,造成了肌腱慢性炎症。受到炎症干扰,肌腱干/祖细胞不再是向着正常的方向(肌腱方向)分化,而是向着骨软骨方向分化,最终形成异位骨化。因此针对肌腱干/祖细胞的异常分化进行早期干预,是保护肌腱免受异位骨化的治疗措施之一。该研究发现mTOR信号通路在肌腱的异位骨化形成中起重要作用,肌腱组织特异mTOR敲除小鼠的肌腱组织异位成骨能力显著减弱,该通路的抑制剂雷帕霉素具备预防肌腱异位骨化的潜力。但肌腱异位骨化一根肌腱的局部病变。因此,需要建立一种具备特异性药物递送功能的载体,能把药物运输至病变部位而不影响其余正常肌腱。鉴于肌腱是一种几乎全部由胶原组成的组织,研究人员选择了胶原杂交肽(Collagen hybridizing peptide, CHP),一种能够特异性结合损伤胶原的多肽。他们利用该种多肽,并结合临床上常用的安全可降解材料聚乳酸-羟基乙酸共聚物(poly(lactic-co-glycolic acid),PLGA,用于包载和缓慢释放药物),制备了一种能够特异性向病理肌腱靶向递送雷帕霉素的材料。研究人员利用该材料,在肌腱损伤的动物模型中成功缓解了肌腱中的异位骨化。
本研究为肌腱损伤治疗找到了一种兼具缓释和靶向功能的新型药物递送材料,并确定了雷帕霉素在肌腱治疗中的作用,为今后肌腱治疗和给药方式提供了新的思路。同时该种材料还具有应用于其他胶原损伤疾病领域研究的可能性。文章发表于《Science Advances》,浙江大学浙二医院骨科学博士陈扬武,浙二医院骨科学肌腱病团队沈炜亮医师为该论文共同第一作者,浙江大学李达三叶耀珍干细胞与再生医学研究中心/浙二医院骨科陈晓教授为通讯作者,浙大高分子系毛峥伟教授,浙江大学基础医学院/浙二医院骨科周以侹教授为共同通讯作者。该工作得到国家重点研发计划和国家自然基金等项目的支持。
原文链接:https://advances.sciencemag.org/content/6/18/eaay9526










