在浩瀚的宇宙中,人类赖以生存的地球大约诞生于46亿年前,地球上最早的生命形式蓝细菌出现于大约35-40亿年前。经过十多亿年的演化,海洋中的蓝细菌开始制造氧气,为其他生命形式的出现提供了基础。我们所知最早的革兰氏阳性肠球菌的出现可追溯至4.5亿年前。从此,地球逐渐被多种细菌统治,从陆地到海洋都遍布细菌的足迹。考古资料显示,地球上人类大约500万年前出现,人类文明的历史仅6000-7000年,可谓时间长河中的‘沧海一粟’。目前地球全部生物量相当于5500亿吨碳,其中细菌和古菌约800亿吨,而包括人类在内的全部动物不足20亿吨。
科学家确定大约有3万多种细菌参与到地球的生态循环系统。人类生活在一个遍布细菌的世界里。正常人的胃肠道所携带细菌数量是我们人体细胞的十倍。在与细菌共存的几百万年历史进程中,我们可能仅仅扮演了一个‘细菌培养皿’的角色。“物竞天择,适者生存”,演化的结果是部分细菌对人体健康有利(比如乳酸菌被用来制备发酵食品和饮料),也有一部分是条件致病菌,会导致传染病,危及人类健康。事实上,我们对细菌的研究仍旧处于初级阶段,许多问题有待解答,例如细菌如何与人类和谐共存?平衡打破后又是如何导致疾病甚至传染性疫情?

猪链球菌包含35种血清型,其中血清二型(SS2)与临床感染密切相关。近年来,二型猪链球菌亦演化为一类新发/再发病原体。该细菌感染对天然宿主猪可引发关节炎/菌血症等疾病,每年给养猪业造成一定的经济损失。此外,该菌可通过伤口入血,对从业人员造成机会性感染,引起脑膜炎甚至链球菌中毒性休克等,病情凶险。在1998与2005年,SS2曾经在我国暴发了二次大规模疫情,造成了数十人死亡。近年来,科学界逐渐达成共识,认为‘细菌脂肪酸的2型合成途径’可开发为一类有潜力的抗菌新靶点。鉴于此,开展与SS2致病机制相关的脂代谢途径研究显得尤为重要。
近日,浙大基础医学院微生物学系冯友军课题组与公共卫生学院周春教授、环境与资源学院逯慧杰研究员深度合作,在动物源性病原体二型猪链球菌的脂肪酸摄取与利用机制方面取得了重要进展。美国东部时间9月2日,题为“Structure and mechanism for streptococcal fatty acid kinase (Fak) system dedicated to host fatty acid scavenging”的研究长文发表于Science旗下刊物Science Advances。该研究成果是继揭示了二型猪链球菌(SS2)的毒力岛89K的播散机制与 NAD+辅酶代谢调控网络可参与SS2致病机制以来,冯友军课题组在二型猪链球菌代谢与感染领域的又一重要进展!
外源性的脂肪酸需要经历‘吸收与活化’加工后,方可被细菌摄取用于膜磷脂的构建,因此脂肪酸的有效摄取是病原体增殖的重要步骤。不同细菌演化出3种脂肪酸摄取机制,分别为:
1.肠杆菌通过内膜蛋白FadD活化脂肪酸生成酯酰基辅酶A,进而进入膜磷脂合成;
2.以弧菌为代表的一类细菌通过AasS将外源脂肪酸转移至ACP载体蛋白,生成酯酰基-ACP进入脂肪酸/膜磷脂/类脂A的途径;
3.包括金黄色葡萄球菌在内的一大类革兰氏阳性细菌编码FakA/FakB二元系统对胞外脂肪酸进行磷酸化,生成‘酯酰基-磷酸’中间体,进而通过PlsX/Y系统参与膜磷脂合成(图1)。
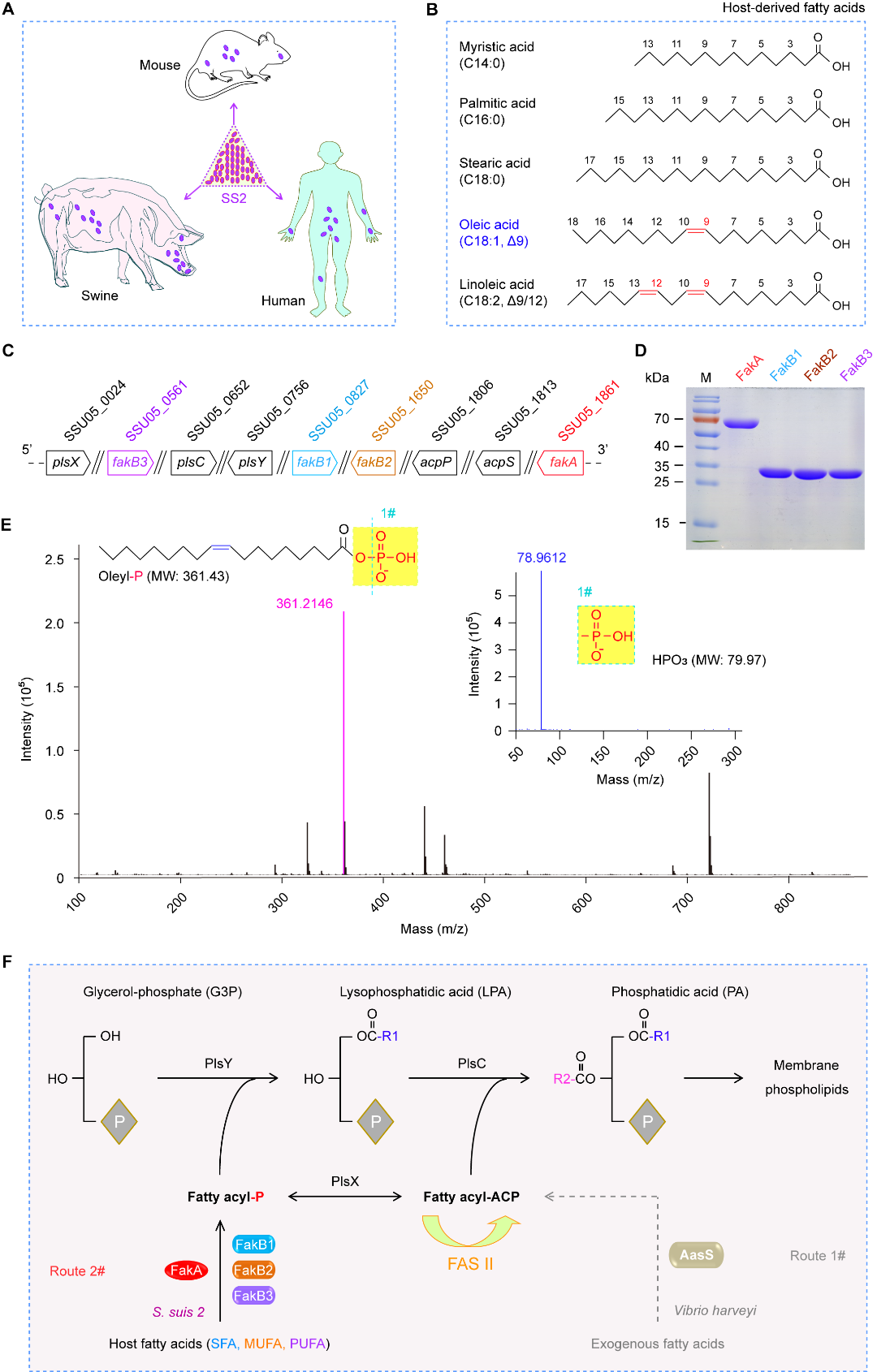
图1 链球菌编码FakA/FakB系统摄取宿主脂肪酸
第三类机制的Fak系统中,FakA是结合ATP的蛋白亚基,FakB负责识别和结合不同类型的脂肪酸(图2)。当FakA与FakB形成功能性复合物后,则具备活化外源性脂肪酸的能力,生成‘脂酰基-磷酸’中间体。近10年来,‘FakA如何识别各种FakB异构体,催化生成多种脂酰基-磷酸的机制’这一关键科学问题一直悬而未决。冯友军课题组利用基因组学手段,发现SS2编码了4套不同的Fak系统,即FakA识别4个FakB亚型(B1至B4)。这提示该病原菌具备多套‘武器装备’,便于其在感染宿主的环境中识别不同种类的宿主脂肪酸并为其所用。
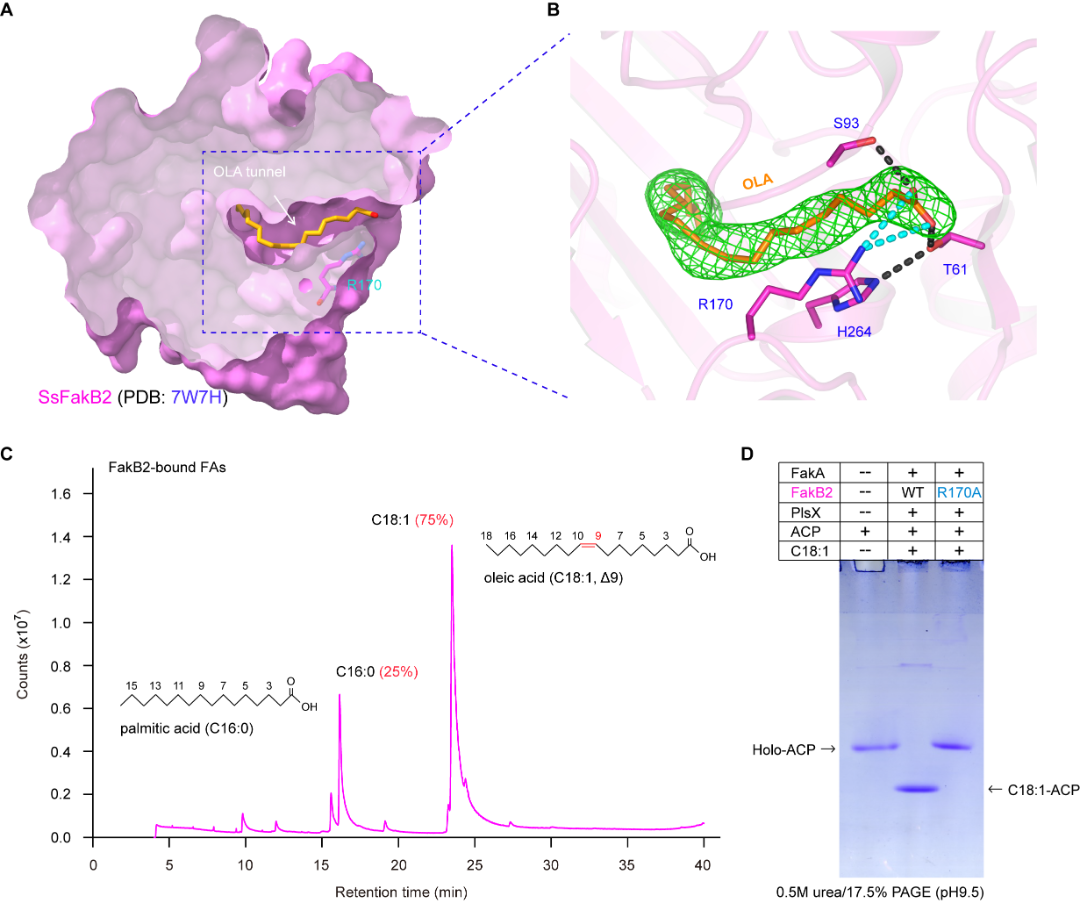
图2 链球菌FakB2识别脂肪酸底物的分子机理
该研究制备了一系列FakA 与FakB蛋白,并建立了一套体外酶学FakA/B-PlsX系统,用于检测‘酯酰基-磷酸’这一反应中间体(图3)。研究团队通过晶体学手段,获得并解析了2.6Å分辨率的FakA/FakB2复合物晶体结构,绘制了FakA二聚体与FakB的识别与装配模型(图3)。通过结构引导的功能突变分析,阐明了FakA/FakB2的互作界面,揭示了FakB2与油酸的识别通道(图2)以及复合物的催化活性中心。该工作首次详尽展示了链球菌用摄取脂肪酸的Fak系统的生化机制(图3),将助力抵御‘烈性链球菌侵袭性感染’的新靶点药物研发。
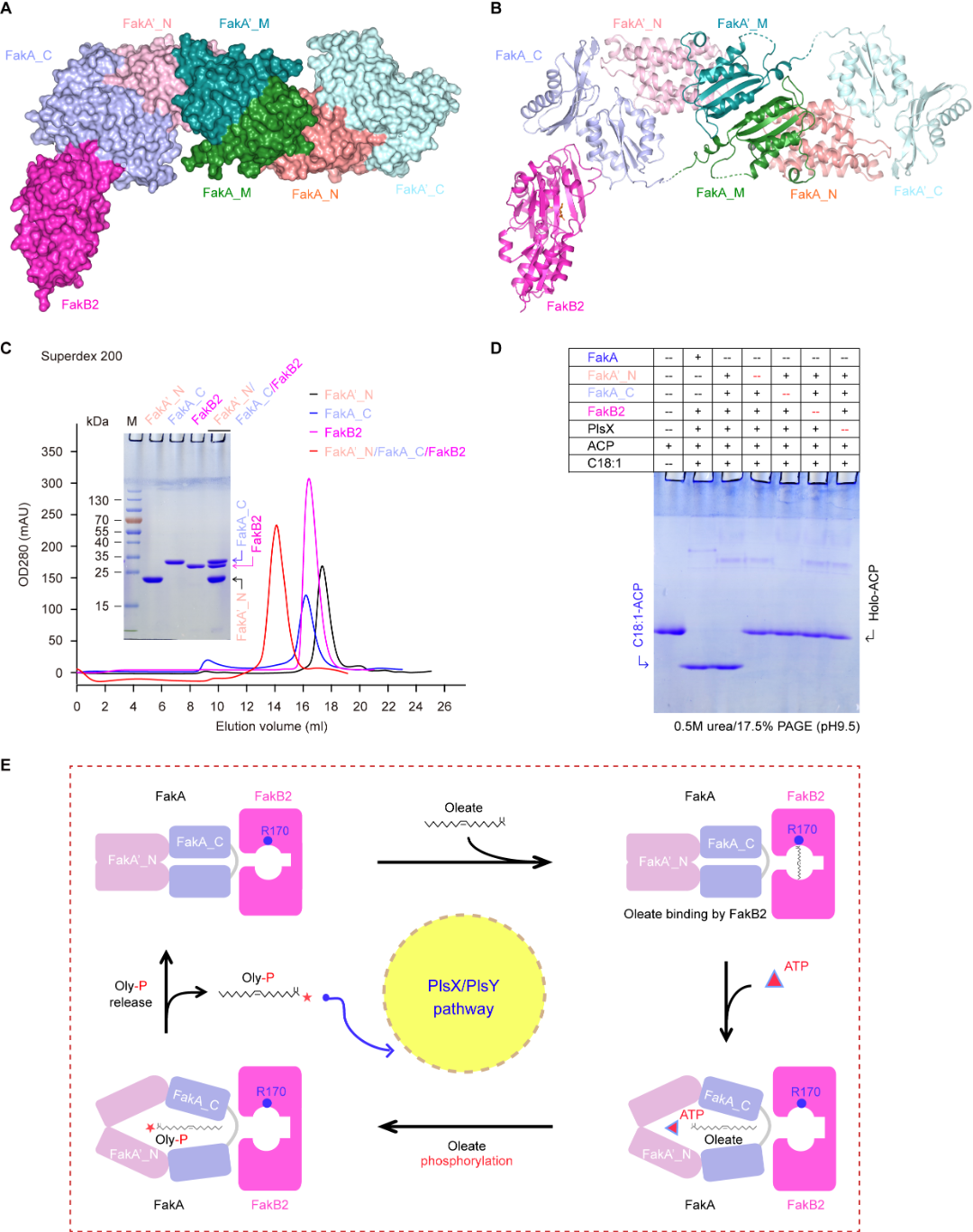
图3 猪链球菌FakA/FakB2的整体结构以其活化脂肪酸的生化机理
冯友军课题组长期聚焦“细菌脂代谢与耐药/致病性的机制”研究,发表重要研究论文60余篇,累计引用9400余次。该研究工作先后获得了国家基金委多个项目的联合资助。
浙江大学基础医学院冯友军课题组硕士生史钰与周春课题组臧宁系该研究论文的共同第一作者。浙江大学基础医学院冯友军教授(https://person.zju.edu.cn/fyj),公共卫生学院周春研究员与环境资源学院逯慧杰研究员担任该研究论文的共同通讯作者。












